職位推薦
- 珍格醫療-臨床銷售 15001-20000
- 地奧制藥-醫藥代表 6001-8000
- 普利德醫療-醫療設備銷售經理 面議
- 大唐-兼職招商經理 面議
- 景德中藥-直營經理 6001-8000
- 安邦醫藥-省區招商經理 8001-10000
- 恒瑞醫藥-醫藥信息溝通專員 6001-8000
- 黃河中藥-學術講師 8001-10000
發布日期:2025-07-18 瀏覽次數:1100
近日,靶向緊密連接蛋白18.2(CLDN18.2)的抗體藥物偶聯物(ADC)SHR-A1904治療晚期胃癌或胃食管結合部癌(GC/GEJC)的研究數據在國際頂級期刊《Nature Medicine》(IF:50.0)正式發表1。該研究成果來自中山大學腫瘤防治中心徐瑞華教授牽頭開展的“注射用SHR-A1904在晚期實體瘤患者中的安全性、耐受性、藥代動力學及療效的開放、單臂、多中心的I期臨床研究”。結果顯示,SHR-A1904在既往接受過治療的CLDN18.2中高表達晚期GC/GEJC患者中表現出令人鼓舞的臨床療效。
01研究背景
胃癌是全球癌癥死亡的主要原因之一2。盡管在一線治療中,化療聯合免疫治療或抗HER2藥物為部分患者帶來了持久的抗腫瘤活性和生存期改善3,4,但HER2高表達人群比例低,且一線治療失敗后的患者預后較差,需探索新的有效治療方案。
CLDN18.2是一種在非惡性胃上皮細胞中表達,且在惡性轉化時暴露于腫瘤細胞表面的緊密連接蛋白5-7,是治療胃癌的極具潛力的治療靶點。然而,既往的CLDN18.2靶向治療策略在抗腫瘤活性和耐藥性方面仍存在局限,亟待更有效的治療手段。
SHR-A1904是由恒瑞醫藥開發的一種新型ADC,由靶向CLDN18.2的單克隆抗體、DNA拓撲異構酶I抑制劑載荷以及可切割肽基連接子構成。其獨特之處在于載荷的選擇,與微管抑制劑不同,這種DNA拓撲異構酶I抑制劑通過不同的機制發揮細胞毒性作用,有望克服既往治療的耐藥性問題。
02研究方法
這是一項SHR-A1904在晚期或轉移性實體瘤患者中的多中心、劑量爬坡、PK拓展和療效拓展的I期臨床試驗。本文報道了SHR-A1904在晚期經治GC/GEJC患者中的研究數據。

圖1 試驗流程8
03研究結果
研究共納入95例CLDN18.2陽性的晚期GC/GEJC患者。所有患者既往都經過了系統治療,其中66(69.5%)例患者接受過兩種或以上系統治療。17(17.9%)例患者的CLDN18.2呈低表達(即1%的腫瘤細胞顯示出1+膜染色強度至<50%的腫瘤細胞顯示出2+/3+強度),78(82.1%)例患者具有中高表達的CLDN18.2(即在≥50%的腫瘤細胞顯示出2+/3+膜染色強度)。
研究期間,患者接受了0.6至8.0 mg/kg每三周一次(Q3W)的SHR-A1904靜脈注射治療(0.6 mg/kg, n=2; 1.2 mg/kg, n=3; 2.4 mg/kg, n=3; 3.6 mg/kg, n=3; 4.8 mg/kg, n=9; 6.0 mg/kg, n=35; 8.0 mg/kg, n=40)。
在劑量遞增階段,SHR-A1904表現出了良好的耐受性。研究選擇6.0mg/kg和8.0mg/kg Q3W繼續在PK拓展和療效拓展階段探索。安全性方面,SHR-A1904在95例患者中的安全性整體可控。
在療效方面,探索性生物標志物分析發現,CLDN18.2表達水平與療效呈正相關,CLDN18.2中高表達的患者對SHR-A1904的治療響應更好。在74例可評估的患者中,1例患者達到完全緩解,25例患者達到部分緩解,客觀緩解率(ORR)為35.1%(95% CI,24.4–47.1),確認的ORR為23.0%(95% CI,14.0–34.2)。在6.0mg/kg和8.0mg/kg兩個劑量組中,確認的ORR分別為26.7%(95% CI,12.3–45.9)和26.5%(95% CI,12.9–44.4);中位緩解持續時間分別為未達到(95% CI,4.2個月–未達到)和8.1個月(95% CI,3.9–未達到)。中位無進展生存期(PFS)在總體人群中為5.6個月(95% CI,4.0–6.9),在6.0mg/kg和8.0mg/kg兩個劑量組中分別為5.6個月(95% CI,3.0–6.9)和5.5個月(95% CI,3.0–8.6)。


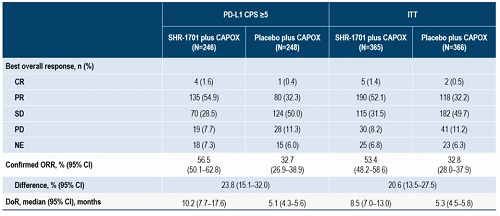
圖2 GC/GEJC患者的最佳總體療效(a)和治療反應的持續時間(b)

圖3 CLDN18.2中高表達GC/GEJC患者的PFS Kaplan-Meier曲線
04研究結論與未來展望
SHR-A1904在既往接受過治療的CLDN18.2中高表達晚期GC/GEJC患者中表現出有前景的臨床療效。SHR-A1904以其差異化的載荷設計和良好的安全性及抗腫瘤活性,有望在未來為晚期GC/GEJC患者提供新的治療選擇。
基于這項I期研究的積極結果,一項SHR-A1904單藥治療的III期臨床試驗(ClinicalTrials.gov,NCT06649292)正在進行中,旨在進一步驗證其二線治療GC/GEJC的療效和安全性。另外,一項Ib/III期臨床試驗(ClinicalTrials.gov,NCT06350006)也在開展中,以探索SHR-A1904聯合治療在一線治療GC/GEJC中的應用潛力。這些后續研究將進一步明確SHR-A1904在胃癌治療中的地位,有望為全球胃癌患者帶來新的希望,改善他們的預后和生活質量。
參考文獻:
1.Ruan, DY. et al. Nat Med (2025). https://doi.org/10.1038/s41591-025-03781-w
2.Bray, F. et al. Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J. Clin. 74, 229–263 (2024).
3.Lordick, F. et al. Gastric cancer: ESMO Clinical Practice Guideline for diagnosis, treatment and follow-up. Ann. Oncol. 33, 1005–1020 (2022).
4.NCCN Clinical Practice Guidelines_Gastric Cancer. 2025. Version 2.2025 — April 4, 2025. https://www.nccn.org/professionals/physician_gls/pdf/gastric.pdf
5.Nakayama, I. et al. Claudin 18.2 as a novel therapeutic target. Nat. Rev. Clin. Oncol. 21, 354–369 (2024).
6.Sahin, U. et al. Claudin-18 splice variant 2 is a pan-cancer target suitable for therapeutic antibody development. Clin. Cancer Res. 14, 7624–7634 (2008).
7.Niimi, T. et al. claudin-18, a novel downstream target gene for the T/EBP/NKX2.1 homeodomain transcription factor, encodes lungand stomach-specific isoforms through alternative splicing. Mol. Cell. Biol. 21, 7380–7390 (2001).
8.Xu, R. H., et al. CLDN18. 2 targeted antibody-drug conjugate (ADC), SHR-A1904, in patients (pts) with gastric/gastroesophageal junction cancer (GC/GEJC): A phase I study." ESMO 2024. Oral presentation, 609O
聲明:
1.本新聞旨在分享學術前沿動態,僅供醫療衛生專業人士基于學術目的參閱,非廣告用途。
2.恒瑞醫藥不推薦任何未被批準的藥品、適應癥的使用。
300多萬優質簡歷
17年行業積淀
2萬多家合作名企業

微信掃一掃 使用小程序

